1.上海市自然科学基金面上项目,20ZR1448700,“分子海绵”circBIRC6的编码功能在DPSCs成牙本质分化中正向调控作用的机制研究。2020/07-2023/06,20万
2.国家自然科学基金青年项目,81300865,组蛋白乙酰化修饰对牙髓细胞成骨/成牙本质分化的调控初探。2014/01-2016/12,23万
课题组成员在牙髓干细胞分化的表观遗传调控及材料促进牙髓-牙本质复合体再生方面取得了良好的课题进展,相关论文发表在FEBS Letter(IF=4.124)、Chem Eng J(IF=13.372)杂志,在工作中获得了本项目的研究灵感,也积累了丰富的工作经验。为开展本课题奠定了扎实的工作基础。指导教师所在课题组团队
项目简介:
目前临床上龋病、牙髓病治疗多使用氢氧化钙、MTA和生物陶瓷类材料,这些材料可控制感染,能在一定程度上实现牙体硬组织的再生,但缺乏促血管、 神经再生的活性。因此,如要实现牙本质-牙髓复合体的再生,所应用的材料应同时具有促牙本质分化、促血管神经形成活性的特点。
氧化石墨烯是石墨烯氧化、剥离的产物,由于其独特的物理化学特性,近年来被广泛应用于药物传递、生物成像及组织工程等领域的研究。因其表面带有大量带负电的含氧官能团如羟基、羧基等,容易与金属阳离子结合。铜离子可介导体内重要的生理活动,参与组织的再生、修复,已有众多研究证实铜离子能够促成骨、成血管及抗菌活性,铜离子可辅助赖氨酰氧化酶催化细胞外胶原的合成;然而含铜离子溶液在体内容易逸散,无法维持有效浓度,高浓度的含铜离子溶液有细胞毒性,需使用控释方法维持铜离子处于相对低浓度以实现生理作用。
课题组前期制备了氧化石墨烯铜纳米颗粒(nGO-Cu)材料,发现其具有促进 hDPSCs 向成牙本质分化的作用,体内实验可见类牙本质-牙髓复合体组织再生(相关成果已发表在顶刊CEJ杂志,Q1,IF=13.273),实验发现nGO-Cu能够促进成牙本质分化相关基因mRNA与蛋白质的表达,促进血管生成及神经生长因子的释放(预初实验1-3)。从材料结构角度看,氧化石墨烯中碳原子sp2、sp3杂化,有共轭大π键,铜元素属于过渡金属第一副族元素,外围价层电子排布为3d104s1,电子迁移活跃,推测对细胞状态、电荷分布有一定影响,具体促进hDPSCs牙髓-牙本质分化的机制有待进一步研究。
正常细胞内线粒体不断进行氧化磷酸化反应,电子转移活跃,双层膜两侧存在电势差,铜离子也是线粒体呼吸酶超氧化物歧化酶、细胞色素C氧化酶的辅酶,推测氧化石墨烯铜这类富电子化合物可一定程度上影响线粒体功能状态。对间充质干细胞来说,未分化状态的细胞以糖酵解供能为主,开始诱导分化后线粒体数量增加,参与氧化磷酸化代谢酶含量增加。线粒体动力学上调频繁,有生成、融合、分裂、转移、自噬等等生理活动,与细胞内其他细胞器关系密切,承担重要的生理功能,前期研究证实hDPSCs成骨诱导条件培养4、7、14天线粒体融合相关基因(OPA1、MFN1、MFN2)、分裂相关基因(FIS1、DRP1)表达上调(预初实验4)。此外,三羧酸循环中一些代谢物(如乙酰CoA等)是染色质修饰酶的底物,可通过控制染色质修饰来调节基因表达,可间接影响干细胞的命运与功能。细胞成骨分化过程中钙离子簇从内质网与磷酸根离子一起被转运至线粒体,随后发生线粒体自噬形成无定形磷酸钙前体,通过基质囊泡排出细胞外,与胶原前体结合一步步形成矿化组织。有研究表明氧化石墨烯可从表观遗传水平降低干细胞相关标志物、增加分化相关标志物的表达。
为了研究氧化石墨烯铜纳米颗粒材料对hDPSCs代谢的影响,课题组进行了以下预实验:利用qRT-PCR检测低浓度nGO-Cu干预3天hDPSCs其线粒体融合(MFN1、OPA1、DRP1)、自噬相关标志物(PINK1、PARKIN)在mRNA水平增加,表观遗传调控相关标志物(SIRT1)在mRNA水平也有增加(预初实验5)。
基于以上信息,我们做出以下科学假设:氧化石墨烯铜纳米材料调控hDPSCs代谢状态:一方面促进线粒体动力学上调,促进线粒体自噬发生,促进钙离子的释放,提高线粒体代谢水平,为hDPSCs定向分化供能;另一方面调控线粒体中间代谢物水平,间接在表观遗传水平上调控hDPSCs的成牙分化。在调控线粒体代谢与表观遗传水平的双重作用下,促进hDPSCs牙髓-牙本质向分化。本研究有望从新角度阐明氧化石墨烯铜等生物富电子化合物可调控线粒体生理活动,进而改变细胞代谢状态与表观遗传水平,促进hDPSCs牙髓-牙本质向分化,为开辟新生物材料提供理论依据与指导。
项目基础:
1、hDPSCs的鉴定
使用改良组织块法培养DPSCs,可见约 2 周后,可见组织块中爬出大量梭形细胞,呈簇状聚集。传代后细胞能够呈长梭形贴壁生长,平均3 天可传代一次(图1a)。成骨诱导 21 天后,茜素红染色阳性。成脂诱导 21 天后,可见细胞呈多层状生长,油红 O 染色呈阳性(图1b)。细胞表达STRO-1,流式细胞仪分析表面标志物显示:第 3 代 DPSCs 表面抗原 CD29 (99.8%)、CD105(83.2%)、CD44(100%)表达阳性,造血干细胞表面抗原 CD31、 CD34、CD45 表达呈阴性(<1%)。(图1c、1d)
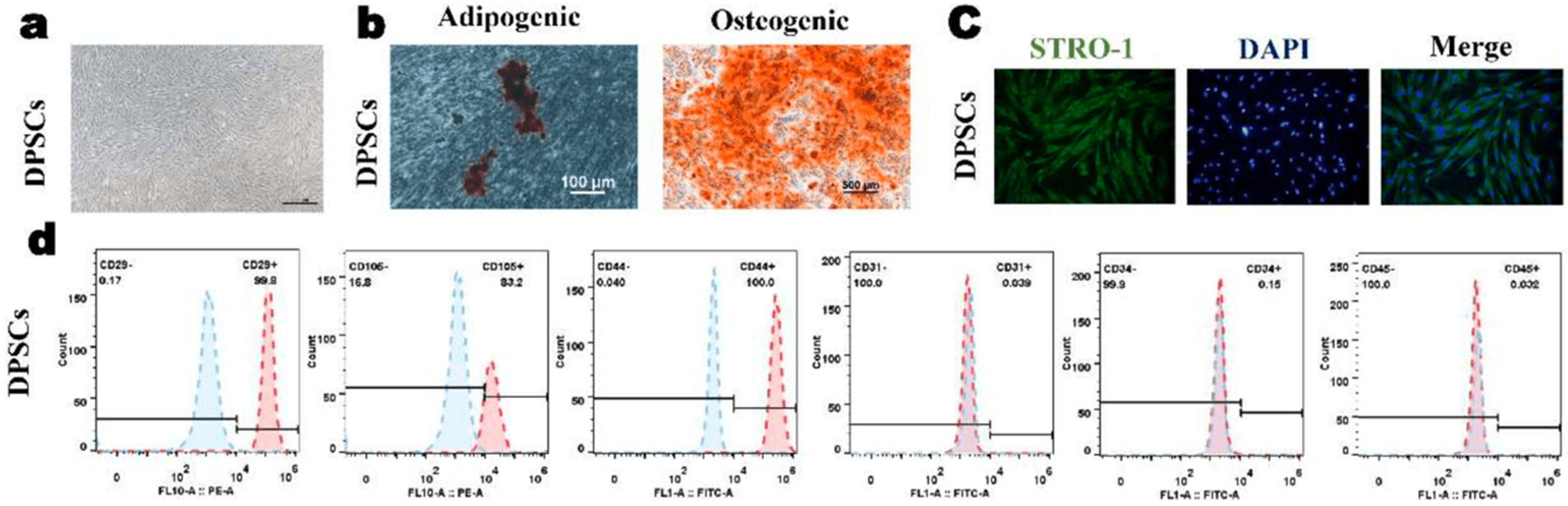
图1 hDPSCs的多向分化能力及免疫表型鉴定。
2、氧化石墨烯铜(GO-Cu)的制备及材料表征

图2 GO-Cu材料的表征。
3、GO-Cu可促进 hDPSCs 成牙本质向分化:
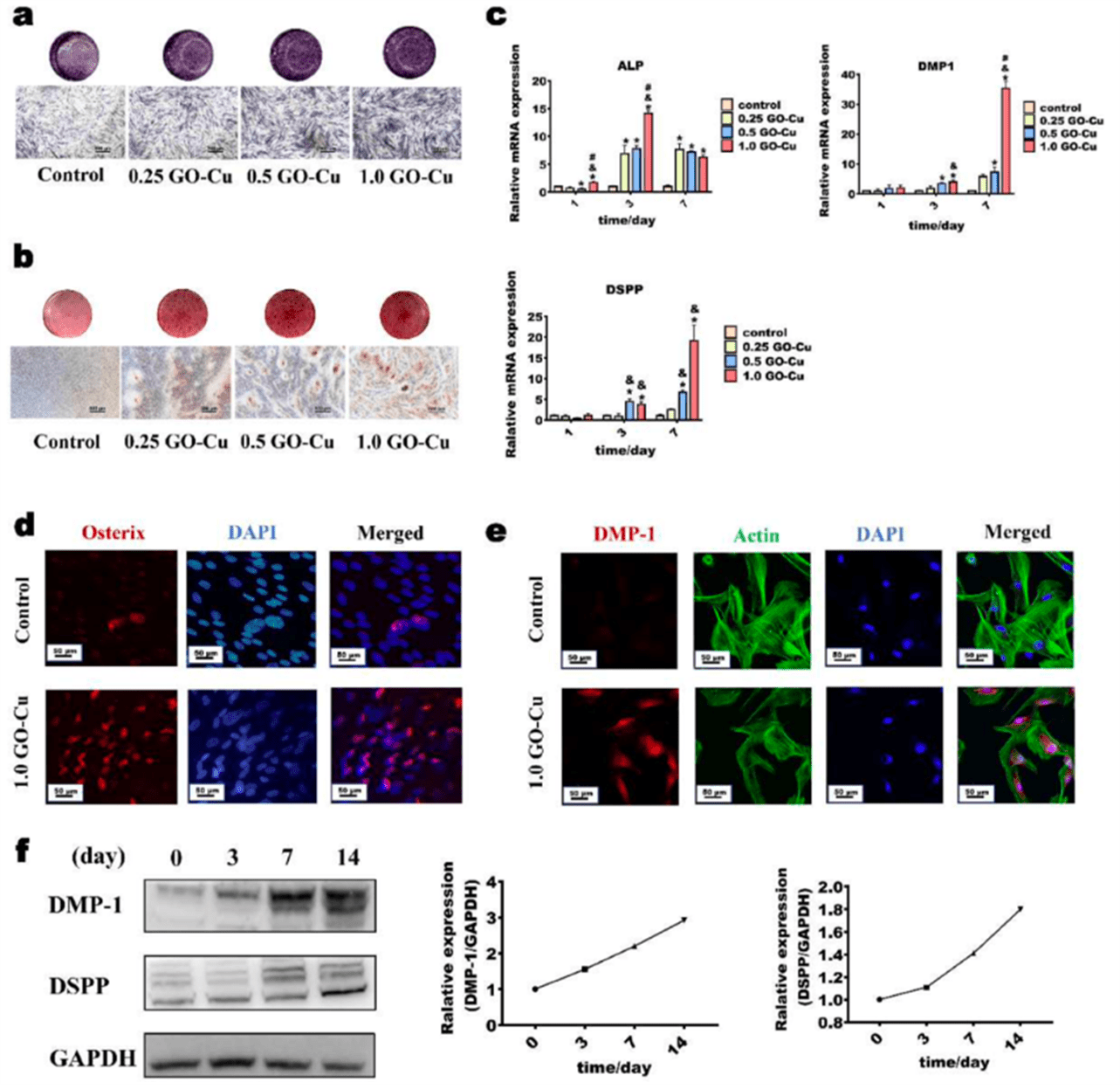
图3 GO-Cu能够促进hDPSCs成牙本质分化。
根据细胞毒性实验的结果,选取了低浓度的 0.25、0.5、1.0 GO-Cu 作用于DPSCs。3 天后进行 ALP 染色,可见实验组较对照组染色深,且染色深度随浓度增加;14天后进行茜素红染色,实验组可见红染的钙结节,且随着浓度增加,钙结节数量亦增加(图3a、3b)。之后进行qRT-PCR,研究GO-Cu 作用于DPSCs后,成牙本质分化相关mRNA的表达变化。共培养 1 天后,实验组 ALP 表达升 高,1.0 GO-Cu 组明显高于其他组;作用 3 天后,实验组 ALP、DMP-1、DSPP 表达水平均上升,其中1.0 GO-Cu组的ALP表达水平达到峰值;作用7天后, ALP表达水平达到稳定,而 DMP-1和DSPP的表达水平,尤其是1.0 GO-Cu组的表达水平进一步上升(图3c)。进一步研究了GO-Cu作用于DPSCs后相关蛋白的变化。免疫荧光染色可见,1.0 GO-Cu 作用于 DPSCs 三天后,转录因子Osterix和成牙本质早期蛋白DMP-1均表达上升(图3d、3e)。Western blot 呈现一致结果,1.0 GO- Cu 作用于 DPSCs 后,DMP-1 和 DSPP的表达量随着作用时间而增加(图3f)。以上结果表明,GO-Cu具有一定的促进DPSCs成牙本质向分化的作用。
4、hDPSCs成牙本质分化过程中线粒体代谢相关基因表达上调。
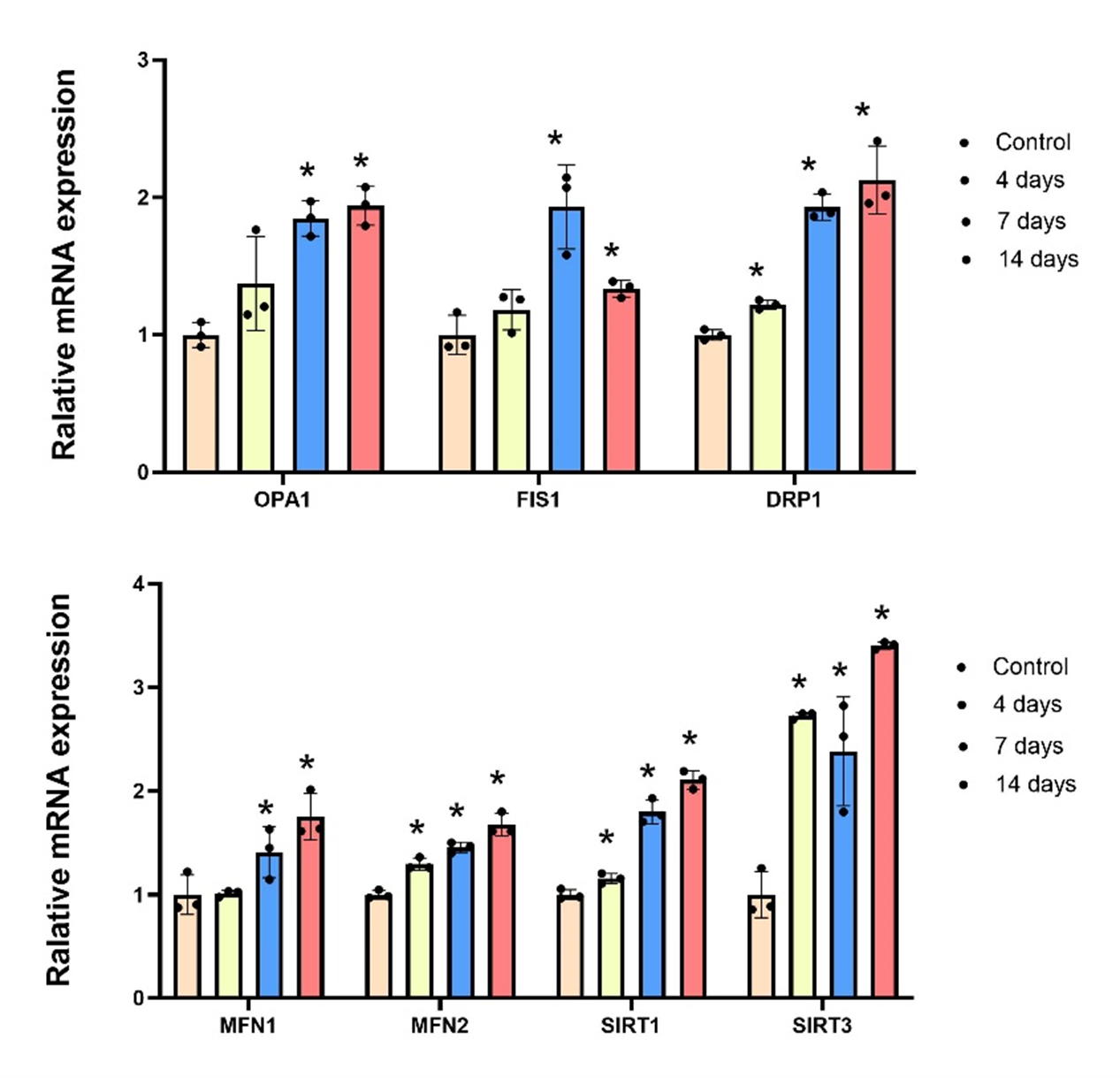
图4 hDPSCs成牙本质诱导后线粒体代谢相关基因的表达情况。
5、GO-Cu影响hDPSCs线粒体代谢水平及表观遗传调控相关酶
我们检测2.5、5、10μg/ml GO-Cu干预3天hDPSCs线粒体融合(MFN1、OPA1、DRP1)在mRNA水平增加(图5a)、自噬相关标志物(PINK1、PARKIN)在mRNA水平增加(图5b),表观遗传调控相关标志物(SIRT1)在mRNA增加(图5c)。
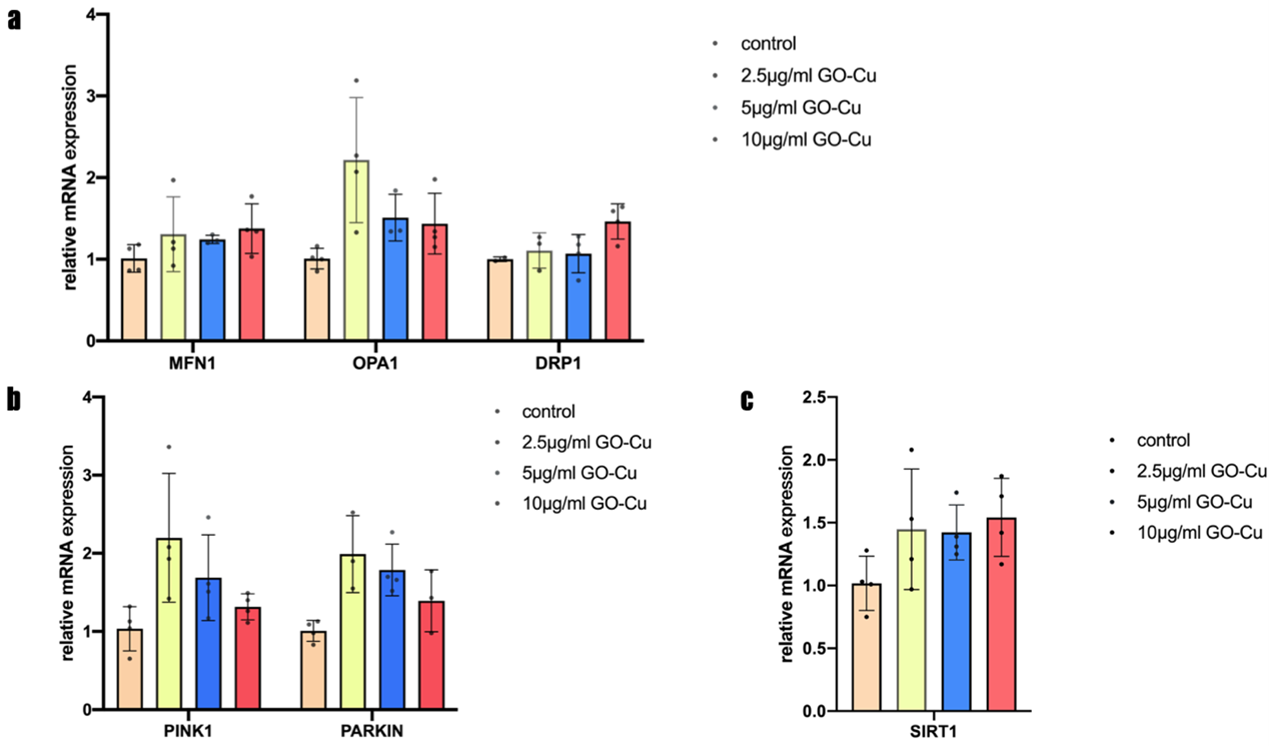
图5 GO-Cu能够上调线粒体动力学及表观遗传相关基因的表达。
预期需要开展的工作:
(1)氧化石墨烯铜材料(GO-Cu)能否在代谢水平调控hDPSCs,促进其牙髓-牙本质分化:
①透射电镜观察GO-Cu干预后3、7、14天hDPSCs中粗面内质网、线粒体、溶酶体等亚细胞结构的改变;
②共聚焦显微镜观察GO-Cu干预后线粒体、溶酶体染色后细胞代谢状态,JC-1染色观察线粒体膜电位变化;
③利用qRT-PCR及WB检测线粒体生成、融合、分裂、自噬、氧化磷酸化酶等相关基因在mRNA水平及蛋白水平的表达情况;
④使用Fura-2-AM荧光钙离子检测试剂盒反映细胞内钙离子的分布;
⑤使用线粒体自噬诱导剂及抑制剂检测其对GO-Cu干预的hDPSCs在mRNA、蛋白水平上线粒体状态及牙髓-牙本质分化的影响。
⑥使用葡萄糖检测试剂盒及ADP/ATP比率检测试剂盒检测GO-Cu干预后hDPSCs的葡萄糖消耗与ATP产生情况,使用Seahorse实时细胞代谢分析检测GO-Cu干预组糖酵解与线粒体呼吸能力变化情况。
(2)氧化石墨烯铜材料(GO-Cu)能否调控线粒体代谢中间产物,间接调控表观遗传水平:
①qRT-PCR、WB检测线粒体氧化磷酸化相关酶的表达;
②试剂盒检测GO-Cu干预情况α-KG、乙酰CoA、SAM等线粒体代谢中间产物水平;
③RNA-seq
检测GO-Cu干预组相关基因表观遗传调控水平。
(3)动物体内氧化石墨烯铜材料(GO-Cu)能否调控hDPSCs线粒体行为:裸鼠皮下埋入去牙髓的牙体硬组织,髓腔内给予不同干预条件,共分3组:空白对照组、hDPSCs组、hDPSCs+GO-Cu组,8周后观察牙髓-牙本质复合体生成情况,制备组织切片,免疫组化法检测组织内线粒体相关标记物的表达情况。
(4)制备新型氧化石墨烯铜材料(GO-Cu):
尝试改变水溶性GO-Cu的形状,使之更适合于临床应用,将hDPSCs与GO-Cu、GelMA混合,在紫外光照射下光固化,形成细胞支架。
①GO-Cu复合光固化水凝胶材料表征:UV-VIS 吸收光谱、扫描电子显微镜、X线衍射分析、机械性能测试(拉伸、压缩)
②体外实验:
使用Live/Dead 细胞染色、CCK-8、黏附蛋白 Integrin-β1 染色等实验检查GO-Cu复合光固化水凝胶材料对hDPSCs活性、增殖、粘附的影响。利用qRT-PCR及WB检测线粒体生成、融合、分裂相关基因在mRNA水平及蛋白水平的表达情况,确定GO-Cu干预后线粒体动力学改变情况
③体内实验:
在裸鼠皮下埋入去处理过的人牙根硬组织,给予不同干预条件,共分3组:空白对照组、GO-Cu复合光固化水凝胶组、GO-Cu复合光固化水凝胶载hDPSCs组;8周后观察牙髓-牙本质复合体形成情况,使用免疫组化方法检测组织内血管神经生成及线粒体相关标记物的表达情况。
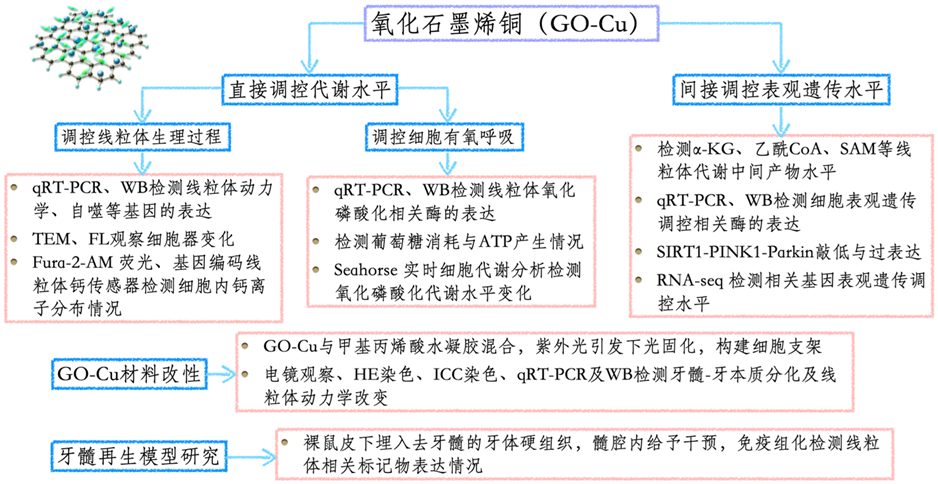
组织路线图:
 大学生创新创业训练计划智能管理平台
大学生创新创业训练计划智能管理平台